深圳子科生物報道:腫瘤特異性的藥物靶向遞送仍是腫瘤治療的難點之一。其中,機體尤其是肝臟巨噬細胞系統對納米藥物的吞噬清除是影響其臨床療效的關鍵因素之一。
日前,由南京醫科大學附屬淮安醫院與美國路易斯維爾大學合作研究發現自體來源的外泌體可有效減少外源性納米藥物被肝臟的吞噬清除,進而提高納米藥物的利用率,實現了納米藥物的靶向再分布,相關研究成果發表于學術期刊Theranostics上。
該項研究中,研究人員首先證實靜脈途徑注射的外泌體及外源性納米藥物載體包括DOTAP:DOPE脂質體等主要分布于小鼠肝臟且均主要被Kupffer細胞所吞噬清除。
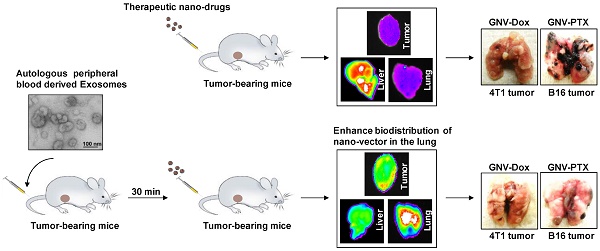
研究同時發現,無論是通過化學制劑Clodrosomes去除肝臟Kupffer細胞還是預先靜脈給予一定劑量的自體外泌體,均可減少外源性納米藥物在小鼠肝臟的分布,實現納米藥物在肺臟及腫瘤部位的再分布;小鼠乳腺癌、黑色素瘤肺轉移模型也進一步證實,足夠劑量的外泌體可有效的減少腫瘤的肺轉移,提高小鼠的生存率。
進一步的機制研究發現,CD36及胰島素樣生長因子1(IGFR 1)受體信號通路在外泌體介導的肝臟Kupffer細胞吞噬抑制作用過程中起到關鍵作用。研究成果為進一步提高納米藥物的利用率提供了新的策略,為腫瘤靶向治療提供了新的思路。




